Der Faber-Castell "VCH Rechenschieber für Chemiker"
Summenformel aus der organischen Element-Analyse
Zu einer Zeit, in der ich Chemie studierte — also zu einer Zeit ohne Taschenrechner oder gar Computer — war eine Elementaranalyse zur Identifikation (organischer) Verbindungen der Standard. Man verbrannte eine kleine Menge (wenige 100 mg) der Substanz, und fing das Kohlendioxid mit Bariumhydroxid als BaCO3 auf und bestimmte dessen Gewicht. Wasserstoff wurde als Wasser in einem Trockenmittel absorbiert und ebenfalls durch Gewichtszunahme bestimmt. Stickstoff wurde als Gas aufgefangen, und dessen Volumen gemessen. Chlor wurde als Silberchlorid gravimetrisch bestimmt, u. s. w.
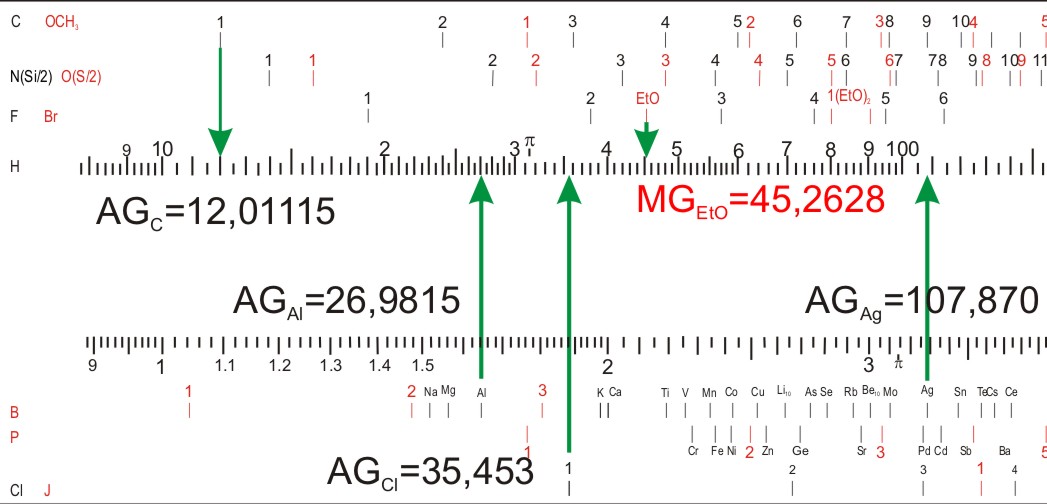
Neben den "üblichen" logarithmischen Skalen sind Markierungen mit Elementsymbolen (C, F, B, P, Cl) und Atomgruppen (OCH3, (EtO)2) auf Körper und Zunge angebracht. Mit den Logarithmen von Elementgewichten und ihren Vielfachen neben den X- und 10·X2-Skalen (die 10·X2-Skala auf dem Körper beginnt mit 10 und endet mit 1.000, die X2-Skalen auf der Zunge beginnt mit 1 und endet mit 100). Die Logarithmen der Elementgewichte korrespondieren mit der 10·X2-Skala.
Oberhalb der 10·X2-Skala findet man die Vielfachen für Kohlenstoff (C, schwarz von 1 bis 80), für Stickstoff (N, schwarz von 1 bis 12) und Silicium/2 (da Si im Rahmen der Ablesegenauigkeit doppelt so schwer ist wie N), und für Fluor (F, schwarz von 1 bis 6). Überlagert sind die Atomgewichte für Sauerstoff (O, rot von 1 bis 12) und Schwefel/2 (da S im Rahmen der Ablesegenauigkeit doppelt so schwer ist wie O), für Brom (Br, rot von 1 bis 6), und für die Atomgruppe Methoxy (OCH3, rot von 1 bis 6). Das Element Wasserstoff (Atomgewicht 1) ist in der X2-Skala der Zunge enthalten, wobei man beim Ablesen auf der X2-Skala auf dem Körper die zehnfache Atommasse einstellen bzw. ablesen muß.
Auf dem unteren Teil des Körpers sind die Logarithmen der Atomgewichte und ihrer Vielfachen von Bor (B, rot von 1 bis 3), Phospor (P, rot von 1 bis 6) Chlor (Cl, schwarz von 1 bis 10) und Iod (J, rot von 1 bis 3) angegeben, sowie die Logaritmen der einfachen Atomgewichte einiger Metalle (schwarz, Elementsymbol am Teilstrich).
Um die Zeit, als der Rechenschieber für Chemiker bei VCH erschien (1971), gab es dann Analysenautomaten, die die prozentualen Atomverhältnisse und das Molekulargewicht in einem Schritt ausgaben. Hier konnte der Rechenschieber für Chemiker dann seine Vorteile ausspielen. Wie man der — recht spärlichen — Anleitung entnimmt, war er vor allem als Hilfsmittel für die organisch-chemischen Analysenberechnungen gedacht. (Anleitung von Gerd Ewald zur Verfügung gestellt.)
Man erhielt von Elementaranalyselabor die Prozent-Angaben:
| Element | Gehalt % |
| C | 34,2 |
| H | 2,1 |
| Br | 38,0 |
| N | 6,0 |
| O | 19,8 |
| MG = 216 | |
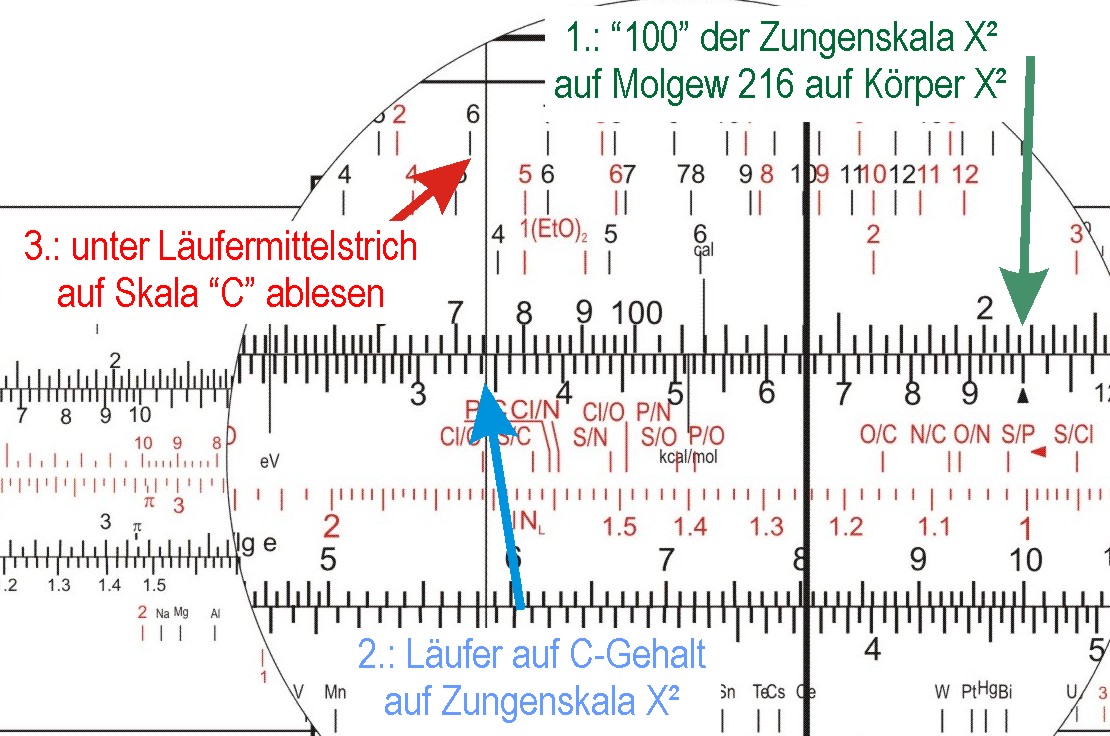
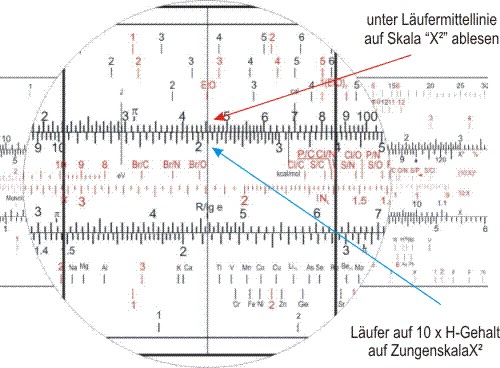
Und sollte nun die Summenformel berechnen. Wohl dem, der einen Rechenschieber für Chemiker hatte! Der stellte die Dreiecksmarke (bei "100" der X2-Skala auf der Zunge unter den Molekulargewichtswert der der X2-Skala auf dem Körper, und schob dann den Läuferstrich auf der Zungenskala X2 über den Prozentwert C. Auf der Skala "C" las man dann 6,2 ab, was etwa 6 C-Atomen entspricht.
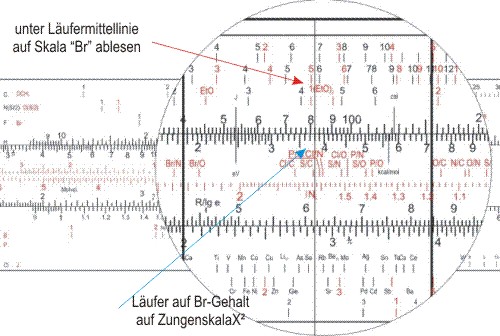
Nun nur den Läufer auf den Bromgehalt schieben und auf der Skala "Br" 1,1 ablesen, was einem Bromatom entspricht.
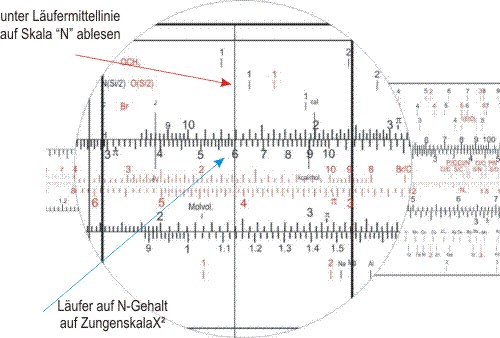
Den Läufer auf den Stickstoffgehalt stellen, und auf der Skala "N" 0,9 ablesen, was einem Stickstoffatom entspricht.
Den Läufer auf den zehnfachen Wert des Wasserstoffgehalts verschieben und auf der X2 des Körpers ablesen 4,52, was 4 oder 5 Wasserstoffatomen entspricht.
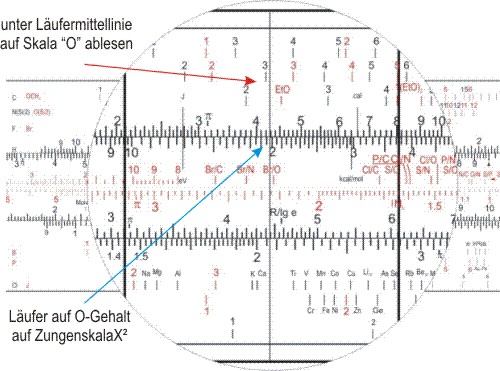
Schließlich schiebt man den Läufer auf den Sauerstoffgehalt und liest 2,7 ab, was drei O-Atomen entspricht.
Es ergeben sich also zwei mögliche Summenformeln: C6H4BrNO3 oder C6H5BrNO3. Nun muß der chemische Sachverstand unterscheiden: C6 deutet auf einen Benzolring hin (C6H6). Das Bromatom ersetzt dann ein Wasserstoffatom (C6H5Br). Bleibt NO3, was auf eine Nitrogruppe (NO2) hinweist, die ein weiteres H-Atom substituiert ⇐ C6H4BrNO2; das verbleibende O-Atom wäre dann eine Phenolgruppe (ersetzt kein H-Atom!). Die wahrscheinliche Summenformel ist also C6H4BrNO3 (Brom-nitro-phenol). Welches der verschiedenen Isomere es ist, bestimmt man z. B. mit dem Schmelzpunkt in dem sich die Isomeren unterscheiden.
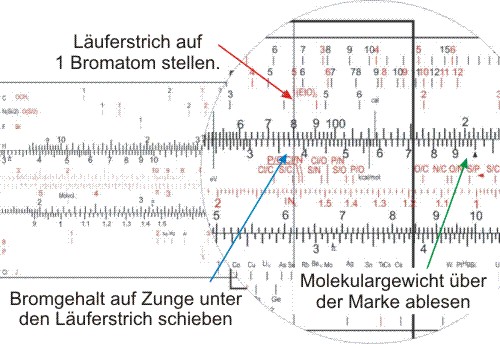
Andersherum kann man aus dem Analyseergebnis auf das Molekulargewicht schließen, wenn man annimmt, die Substanz enthält nur ein Bromatom. Man stellt den Läuferstrich auf den Logarithmus des Atomgewichts von Brom, schiebt der Wert des Analyseergenisses auf der Zunge unter den Läuferstrich und liest über der "MG"-Marke das Molekulargewicht ab: 212.
Natürlich kann man aus der Summenformel und dem sich daraus errechnenden Molekulargewicht auch die prozentuale Elementzusammensetzung berechnen. Nehmen wir z. B. Frigen 113 C2F3Cl3.
| Element | Symbol | Atomgewicht | Gehalt (%) |
| Kohlenstoff | C | 12,000 | 12,8 |
| Fluor | F | 18,998 | 30,4 |
| Chlor | Cl | 35,45 | 57,1 |
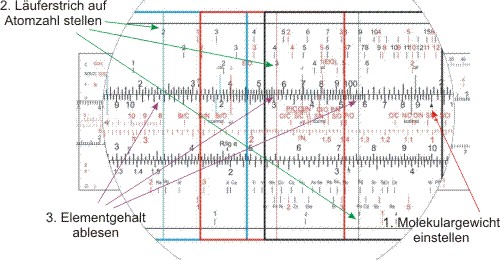
Das Molekulargewicht ist 187,34. Unter diese Zahl auf der X2-Skala des Körpers stellt man die "MG"-Marke der X2-Skala auf der Zunge. Dann braucht man nur noch den Läufer nacheinander auf die Atomzahl der Skala des entsprechenden Elements zu verschieben und liest jedesmal den Prozentgehalt des Elements auf der X2-Skala der Zunge ab.
Im Prinzip könnte man das auch mit dem Taschenrechner ausrechnen, aber leichter — durch dreimaliges Verschieben des Läufers — geht es mit dem Rechenschieber.
Themen
[Einleitung]
[Faber-Castell]
[Nestler 33]
[chemisches Rechnen]
[Periodensystem]
[Vorproben]
[Quantitative Analyse]
[Stöchiometrische Tafel]