Der Rechenschieber für Chemiker
Übersicht
Unter den vielen Sonderausführungen von Rechenschiebern ist der "Rechenschieber für Chemiker" einer der Exoten. Trotzdem haben wohl die meisten namhaften Hersteller ein Modell für Chemiker angeboten. Unter Chemikern — genauer unter Analytikern — waren diese Rechenschieber aber seit Anfang des 19. Jahrhundert wohl sehr beliebt. Ich habe zwei Modelle: den Nestler Chemiker 33 (Patent von 1910) und den von Faber-Castell (Vertrieb durch Verlag Chemie (Weinheim), 1970).
Der Nestler Chemie ist für die anorganische Elementanalyse optimiert. Er weist starke Gebrauchsspuren auf, die Skalenlänge beträgt 25 cm, die Zunge hat Skalen auf beiden Seiten:
Der Faber-Castell (Skalenlänge 12,5 cm) ist für die organisch-chemische Analyse optimiert. Meiner ist fabrikneu. Auf der einen Seite sieht er wie ein gewöhnlicher Rechenschieber aus:
Auf der anderen fallen Elementsymbole auf:
Ich gebe zu: ich hatte keinen Spezialrechenschieber, solange ich Chemiker war (und brauchte ihn wohl auch nicht). Erst als ich die Anfrage erhielt: "Ich habe da einen Rechenschieber für Chemiker. Wie verwendet man den?" erinnerte ich mich und bekam tatsächlich einen von Herrn Peter Holland, der auch die Website der Rechenschiebersammler betreute.
Die Rechenschieber für Chemiker fallen vor allem durch zusätzliche Skalen auf dem Körper und der Zunge mit Elementsymbolen und Atomgruppen auf — das liegt daran, dass für Chemiker die Elemente mit einer Fülle Eigenschaften verbunden sind. Jedes Element tritt nach bestimmten Regeln (und ihren Ausnahmen) mit anderen Elementen zusammen und bildet Verbindungen. Die für das Rechenschieberrechnen entwickelte Regelwerk heißt "Stöchiometrie"; es füllt Bände. Mit dem Rechenschieber für Chemiker erfolgreich umzugehen, braucht es "vertiefte Kenntnisse chemischer Zusammenhänge", sagt Walter Wittenberger, einer der Päpste.
Das geht mir zu weit. Ich will nur an wenigen Beispielen den prizipiellen Einsatz zeigen. Wer es wirklich will, kann ein paar Grundlagen nachlesen. Oder sich über den Ablauf einer quantitativen Analyse informieren. Da von den chemischen Symbolen der Faber-Castell für die organisch-chemische, und der Nestler für die anorganisch-chemische Analyse konzipiert scheint, soll je ein Beispiel den Gebrauch veranschaulichen.
Rechenschieber für Chemiker Anleitungen im Web:
- Keuffel & Esser Co., New York: The Chemist′s Duplex Slide Rule.
- Unique Slide Rule Company Brighton: Instruction Leaflet for Unique Chemical Slide Rule
Der Faber-Castell (VCH) "Rechenschieber für Chemiker"
Summenformel aus der organischen Element-Analyse
Zu einer Zeit, in der ich Chemie studierte — also zu einer Zeit ohne Taschenrechner oder gar Computer — war eine Elementaranalyse zur Identifikation (organischer) Verbindungen der Standard. Man verbrannte eine kleine Menge (wenige 100 mg) der Substanz, und fing das Kohlendioxid mit Bariumhydroxid als BaCO3 auf und bestimmte dessen Gewicht. Wasserstoff wurde als Wasser in einem Trockenmittel absorbiert und ebenfalls durch Gewichtszunahme bestimmt. Stickstoff wurde als Gas aufgefangen, und dessen Volumen gemessen. Chlor wurde als Silberchlorid gravimetrisch bestimmt, u. s. w.
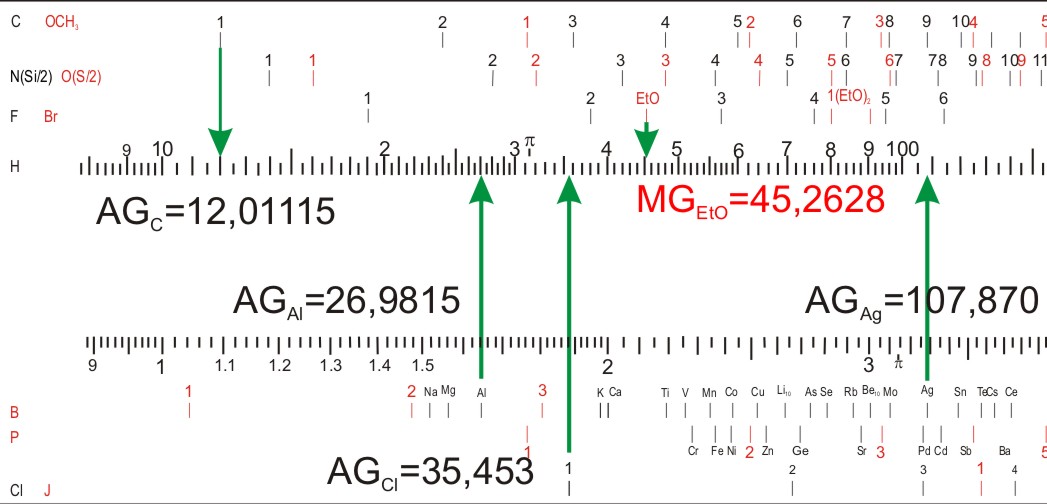
Neben den "üblichen" logarithmischen Skalen sind Markierungen mit Elementsymbolen (C, F, B, P, Cl) und Atomgruppen (OCH3, (EtO)2) auf Körper und Zunge angebracht. Mit den Logarithmen von Elementgewichten und ihren Vielfachen neben den X- und 10·X2-Skalen (die 10·X2-Skala auf dem Körper beginnt mit 10 und endet mit 1.000, die X2-Skalen auf der Zunge beginnt mit 1 und endet mit 100). Die Logarithmen der Elementgewichte korrespondieren mit der 10·X2-Skala.
Oberhalb der 10·X2-Skala findet man die Vielfachen für Kohlenstoff (C, schwarz von 1 bis 80), für Stickstoff (N, schwarz von 1 bis 12) und Silicium/2 (da Si im Rahmen der Ablesegenauigkeit doppelt so schwer ist wie N), und für Fluor (F, schwarz von 1 bis 6). Überlagert sind die Atomgewichte für Sauerstoff (O, rot von 1 bis 12) und Schwefel/2 (da S im Rahmen der Ablesegenauigkeit doppelt so schwer ist wie O), für Brom (Br, rot von 1 bis 6), und für die Atomgruppe Methoxy (OCH3, rot von 1 bis 6). Das Element Wasserstoff (Atomgewicht 1) ist in der X2-Skala der Zunge enthalten, wobei man beim Ablesen auf der X2-Skala auf dem Körper die zehnfache Atommasse einstellen bzw. ablesen muß.
Auf dem unteren Teil des Körpers sind die Logarithmen der Atomgewichte und ihrer Vielfachen von Bor (B, rot von 1 bis 3), Phospor (P, rot von 1 bis 6) Chlor (Cl, schwarz von 1 bis 10) und Iod (J, rot von 1 bis 3) angegeben, sowie die Logaritmen der einfachen Atomgewichte einiger Metalle (schwarz, Elementsymbol am Teilstrich).
Um die Zeit, als der Rechenschieber für Chemiker bei VCH erschien (1971), gab es dann Analysenautomaten, die die prozentualen Atomverhältnisse und das Molekulargewicht in einem Schritt ausgaben. Hier konnte der Rechenschieber für Chemiker dann seine Vorteile ausspielen. Wie man der — recht spärlichen — Anleitung entnimmt, war er vor allem als Hilfsmittel für die organisch-chemischen Analysenberechnungen gedacht. (Anleitung von Gerd Ewald zur Verfügung gestellt.)
Rechenbeispiel 1
Man erhielt von Elementaranalyselabor die Prozent-Angaben:
| Element | Gehalt % |
| C | 34,2 |
| H | 2,1 |
| Br | 38,0 |
| N | 6,0 |
| O | 19,8 |
| MG = 216 | |
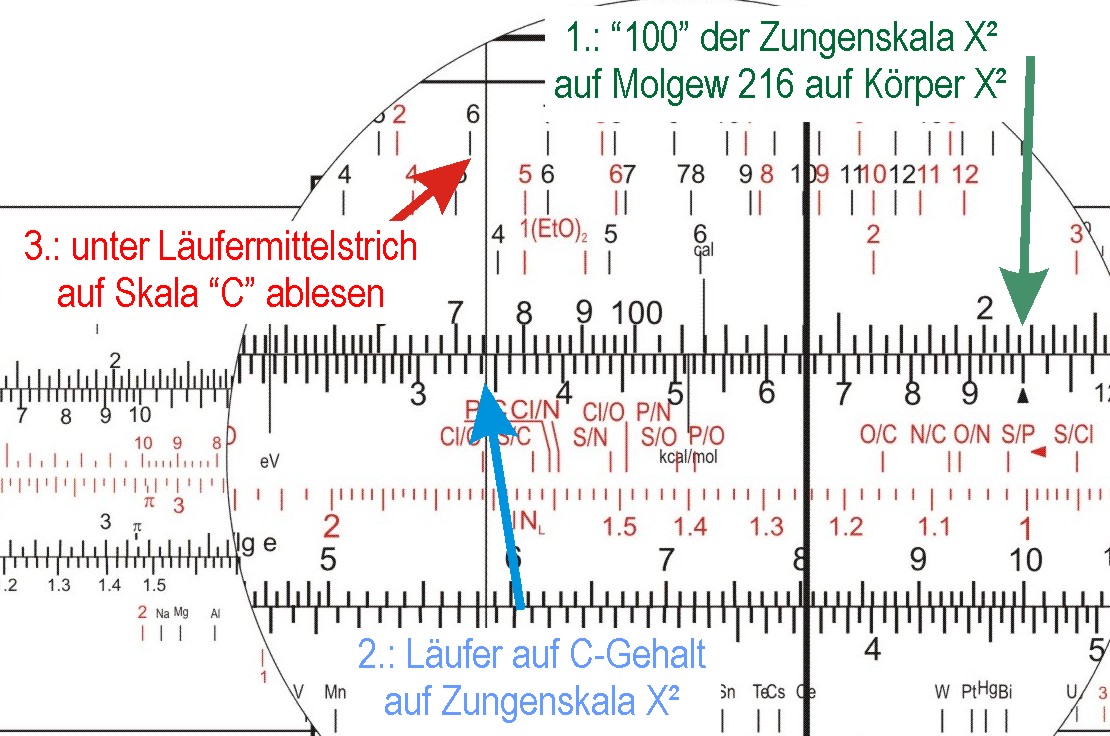
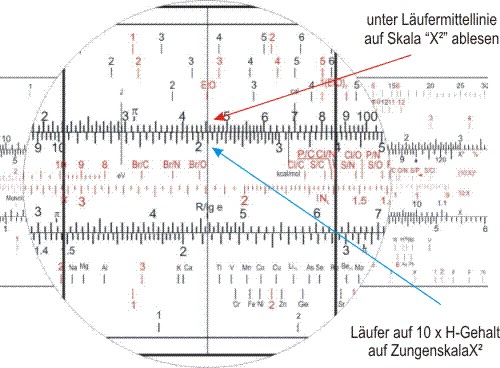
Und sollte nun die Summenformel berechnen. Wohl dem, der einen Rechenschieber für Chemiker hatte! Der stellte die Dreiecksmarke (bei "100" der X2-Skala auf der Zunge unter den Molekulargewichtswert der der X2-Skala auf dem Körper, und schob dann den Läuferstrich auf der Zungenskala X2 über den Prozentwert C. Auf der Skala "C" las man dann 6,2 ab, was etwa 6 C-Atomen in der Summenformel entspricht.
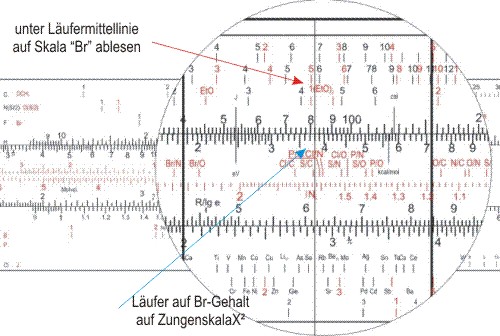
Nun nur den Läufer auf den Bromgehalt schieben und auf der Skala "Br" 1,1 ablesen, was einem Bromatom in der Summenformelentspricht.
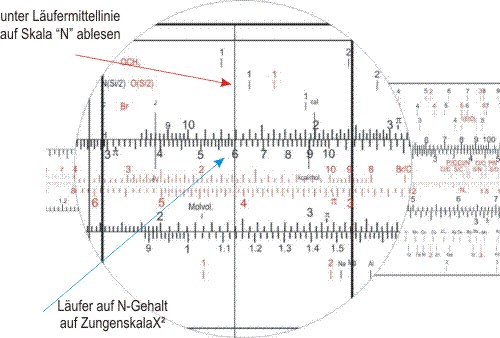
Den Läufer auf den Stickstoffgehalt stellen, und auf der Skala "N" 0,9 ablesen, was einem Stickstoffatom in der Summenformel entspricht.
Den Läufer auf den zehnfachen Wert des Wasserstoffgehalts verschieben und auf der X2 des Körpers ablesen 4,52, was 4 oder 5 Wasserstoffatomen in der Summenformel entspricht.
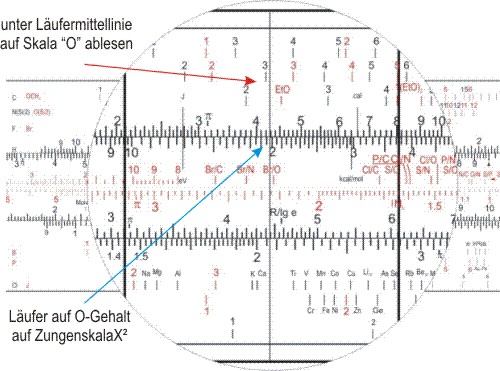
Schließlich schiebt man den Läufer auf den Sauerstoffgehalt und liest 2,7 ab, was drei O-Atomen in der Summenformel entspricht.
Es ergeben sich also zwei mögliche Summenformeln: C6H4BrNO3 oder C6H5BrNO3. Nun muß der chemische Sachverstand unterscheiden: C6 deutet auf einen Benzolring hin (C6H6). Das Bromatom ersetzt dann ein Wasserstoffatom (C6H5Br). Bleibt NO3, was auf eine Nitrogruppe (NO2) hinweist, die ein weiteres H-Atom substituiert ⇐ C6H4BrNO2; das verbleibende O-Atom wäre dann eine Phenolgruppe (ersetzt kein H-Atom!). Die wahrscheinliche Summenformel ist also C6H4BrNO3 (Brom-nitro-phenol). Welches der verschiedenen Isomere es ist, bestimmt man z. B. mit dem Schmelzpunkt in dem sich die Isomeren unterscheiden.
Rechenbeispiel 2
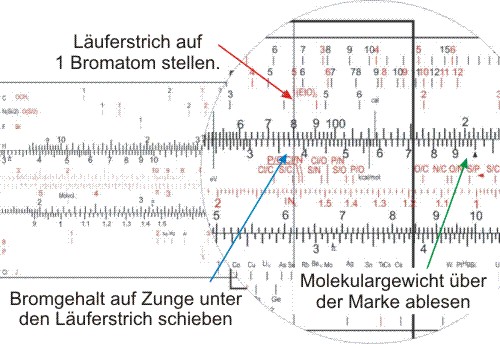
Andersherum kann man aus dem Analyseergebnis auf das Molekulargewicht schließen, wenn man annimmt, die Substanz enthält nur ein Bromatom. Man stellt den Läuferstrich auf den Logarithmus des Atomgewichts von Brom, schiebt der Wert des Analyseergenisses auf der Zunge unter den Läuferstrich und liest über der "MG"-Marke das Molekulargewicht ab: 212.
Natürlich kann man aus der Summenformel und dem sich daraus errechnenden Molekulargewicht auch die prozentuale Elementzusammensetzung berechnen. Nehmen wir z. B. Frigen 113 C2F3Cl3.
| Element | Symbol | Atomgewicht | Gehalt (%) |
| Kohlenstoff | C | 12,000 | 12,8 |
| Fluor | F | 18,998 | 30,4 |
| Chlor | Cl | 35,45 | 57,1 |
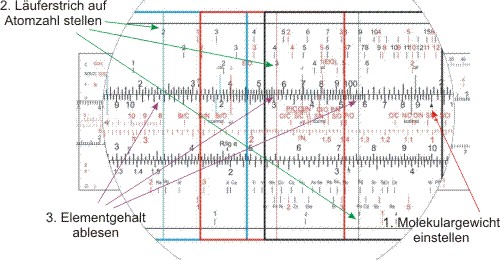
Das Molekulargewicht ist 187,34. Unter diese Zahl auf der X2-Skala des Körpers stellt man die "MG"-Marke der X2-Skala auf der Zunge. Dann braucht man nur noch den Läufer nacheinander auf die Atomzahl der Skala des entsprechenden Elements zu verschieben und liest jedesmal den Prozentgehalt des Elements auf der X2-Skala der Zunge ab.
Im Prinzip könnte man das auch mit dem Taschenrechner ausrechnen, aber leichter — durch dreimaliges Verschieben des Läufers — geht es mit dem Rechenschieber.
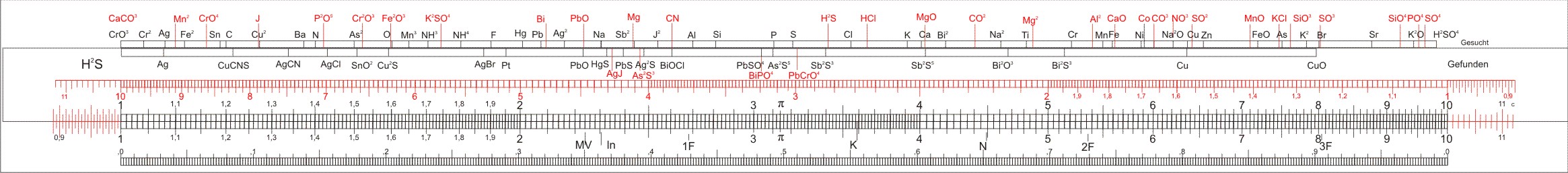
Der "Nestler Chemiker Nr. 33"
Anders als die organisch-chemische Analyse, die auf ein paar Elemente beschränkt ist (fast ausschließlich Kohlenstoff C, Wasserstoff H und Sauerstoff O), beschäftigt sich die anorganisch-chemische Analyse mit den restlichen etwa 100 Elementen. Deren quantitative Bestimmung in Mineralien, Umweltproben, u. s. w., kann sehr anspruchsvoll sein.
Der Nestler Chemie Nr. 33 war auf die quantitative anorganische Analytik optimiert — anders als der Faber-Castell. Er wurde wohl um 1925 hergestellt, wie man am Atomgewicht für Stickstoff (N) von 14,008 und dem für Kohlenstoff (C) von 12,00 auf der Rückseite des Körpers durch Vergleich mit der historischen Entwicklung der Atomgewichte schließen kann.
Die chemischen Markierungen
Der obere Teil des Körpers trägt Markierungen mit chemischen Symbolen (der Übersicht halber sind einige rot). Bezogen auf logarithmische Skala im unteren Teil stellen die Markierungen das Molekulargewicht dar (bzw. dessen Logarithmus).
| CaCO3 | CrO3 | Cr2 | Ag | Mn2 | Fe2 | CrO4 | Sn | C | Cu2 |
| J | Ba | N | P2O5 | As2 | Cr2O3 | O | Fe2O3 | Mn3 | NH3 |
| KSO4 | NH4 | F | Hg | Pb | Bi | Ag2 | PbO | Na | Sb2 |
| Mg | J2 | CN | Al | Si | P | S | H2S | Cl | HCl |
| K | Ca | MgO | Bi2 | CO2 | Na2 | Ti | Mg2 | Cr | Al2 |
| Mn | Fe | CaO | Ni | Co | CO3 | Na2O | NO3 | Cu | SO2 |
| Zn | MnO | FeO | KCl | As | SiO3 | K2 | SO3 | Br | Sr |
| SiO4 | K2O | PO4 | SO4 | H2SO4 | |||||
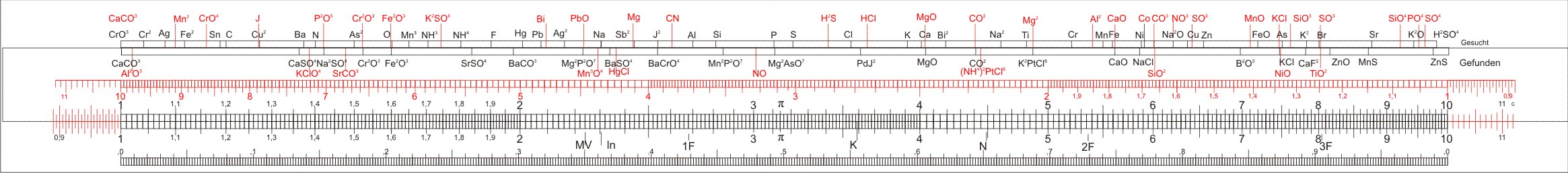
Die Zunge hat ähnliche Markierungen, allerdings unterschiedliche auf Vorder- und Rückseite.
| CaCO3 | Al2O3 | CaSO4 | KClO4 | Na2SO4 | SrCO3 | Cr2O3 | Fe2O3 | SrSO4 | BaCO3 |
| Mg2P2O7 | Mn3O4 | HgCl | BaSO4 | BaCrO4 | Mn2P2O7 | NO | Mg2As2O7 | CO2 | (NH4)2PtCl6 |
| K2PtCl6 | CaO | NaCl | SiO2 | B2O3 | KCl | NiO | CaF2 | TiO2 | ZnO |
| MnS | ZnS | ||||||||
| Ag | CuCNS | AgCN | AgCl | SnO2 | Cu2S | AgBr | Pt | PbO | HgS |
| AgJ | PbS | As2S3 | Ag2S | BiOCl | Sb2S3 | Bi2O3 | Cu | CuO | |
Diese Skalen mit Atomgruppen und Verbindungen gehen auf William Hyde Wollastons Synoptic Scale of Equivalents zurück. Sie bilden im Grunde das Gesetz der konstanten Proportionen (1797 von Joseph-Louis Proust aufgestellt) ab, wonach die Elemente in einer stabilen chemischen Verbindung immer im gleichen Verhältnis vorkommen.
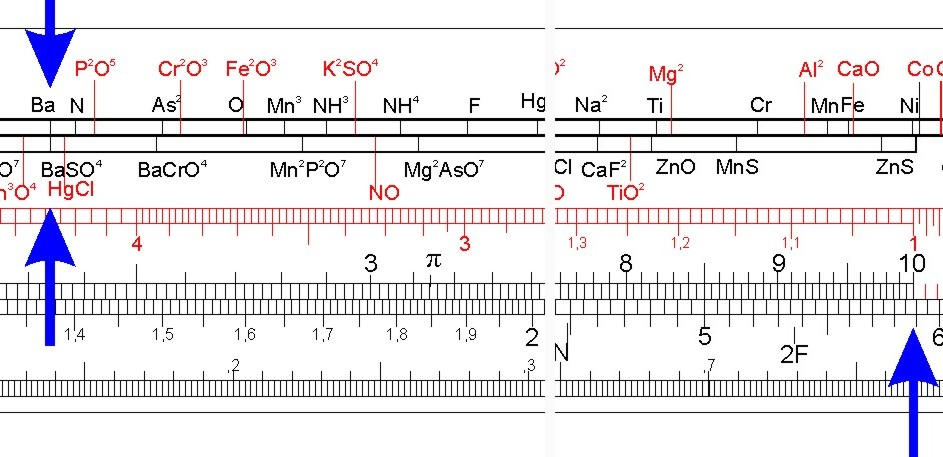
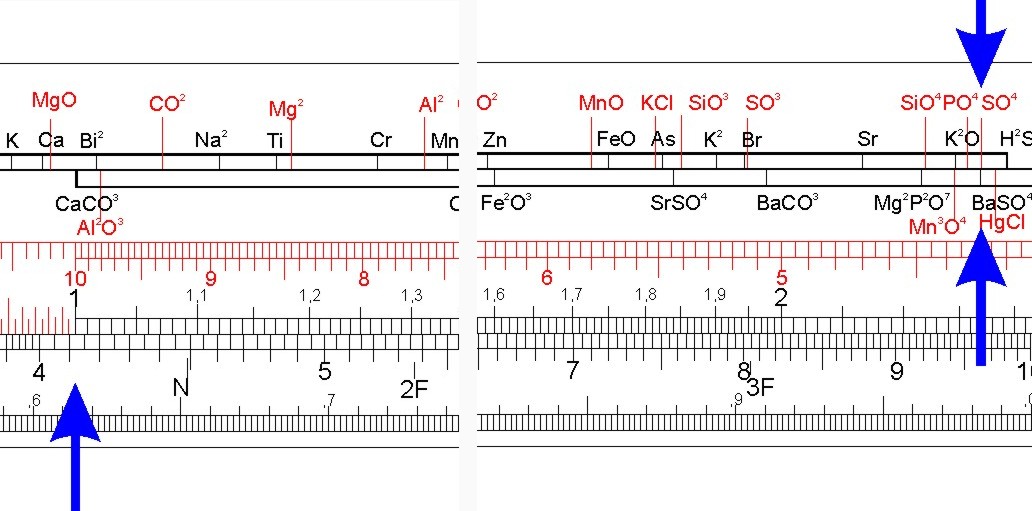
Die Verbindung Bariumsulfat (BaSO4) besteht also aus Barium (Ba) und dem Sulfatanion (SO4-2) im Verhältnis 1 : 1. Da Chemiker gerne und sehr genau wägen, interessiert sie das Gewichtsverhältnis der Bestandteile:
- MGBa = 137,3 g,
- MGSO4 = MGS + 4 · MGO = 32 g + 64 g = 96 g,
- also:
- MGBaSO4 = 137 g + 96 g = 233 g.
- 100 g Bariumsulfat enthalten damit:
- (137 g ⁄ 233) · 100 = 58,8 % Barium und
- (96 g ⁄ 233) g · 100 = 41,2 % Sulfationen.
Dieses Verhältnis ist für jede Menge Bariumsulfat konstant.
Man findet es mit dem Nestler Chemiker 33:
Weitere Markierungen
Auf dem unteren Teil des Körpers sind noch die Markierungen MV, ln, 1F, K, N, 2F und 3F angebracht. Sie dienen zur Vereinfachung spezieller Analysemethoden.
- MV = 22,4. Molvolumen der Gase.
- ln = 2,27. Eulersche Zahl.
- 1F = 26,8 A · h. Zur Bestimmung der Menge a elekrolytisch abgeschiedener Elemente
- a = (Atomgewicht ⁄ nF) · Strommenge.
- K = 273 ⁄ 760 = 0,3592. Reduktionskonstante für Gasvolumina auf Normalbedingungen.
- N = 273 ⁄ 760 · 0,0012505 =0,004491. K · ρN, zur direkten Bestimmung des Gewichts eines aufgefangenen Stickstoffvolumens.
- 2F, 3F: Vielfache von 1F, zur elektrolytischen Bestimmung mehrwertiger Metalle.
Bestimmung von Chlorid
Das Beispiel einer quantitativen Bestimmung von Chlorid soll ein Schritt eines Analyseablaufs sein.
Bei einer Chloridbestimmung betrug die Einwaage s = 0,520 g, erhalten wurde als Niederschlag a = 0,370 g AgCl. Gesucht: g und % Cl in der Substanzeinwaage s.
- g Cl = (Cl ⁄ AgCl) · a
- % Cl = (Cl ⁄ AgCl) · (a ⁄ s) · 100
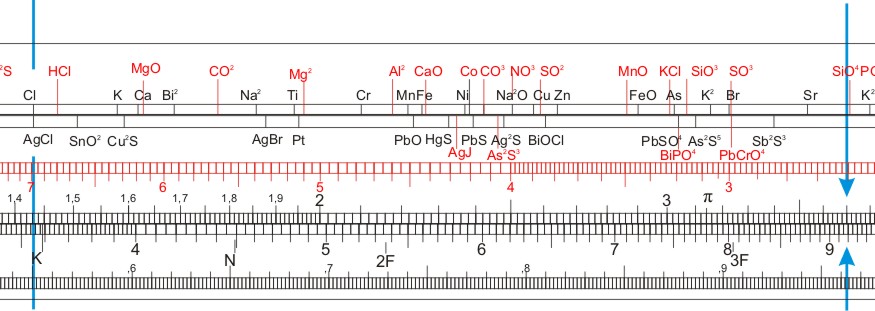
Die Lösung findet man mit der AgCl-Marke der Zunge unter der Cl-Marke auf dem Körper durch verschieben des Läufers auf 0,370 auf der Zunge. Nun liest man auf dem Körper ab: g Cl = 0,0916 g.
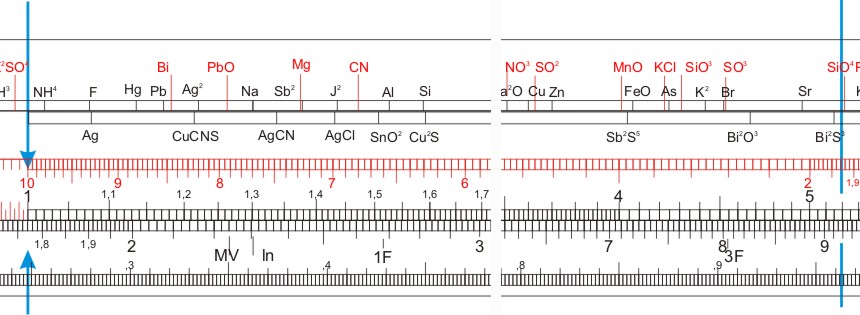
Verschiebt man nun die Zunge, sodass s = 0,520 g unter dem Läuferstrich steht, liest unter der 1 auf der Zunge ab: % Cl = 17,6 %.
Chemisches Rechnen
Die Chemie ist die Wissenschaft von der Materie, ihrer Zusammensetzung und der (gezielten) Veränderung ihrer Bestandteile. Zur Beschreibung der Materie benutzt man das Konzept der "Atome", die nach Regeln zu "Molekülen" zusammentreten. Atome und Molekülen lagern sich zur "Materie", die man anfassen kann, zusammen.
Gemeinerweise gehorchen die Atome beim Bilden von Verbindungen zwar allgemeinen Regeln, aber es gibt einige hundert Millionen Verbindungen, zu denen die Atome zusammentreten können. Die beiden Elemente Natrium (Na) und Chlor (Cl) bilden miteinander Kochsalz (NaCl), in dem je ein Atom Natrium und Chlor enthalten sind:
- Na + Cl = NaCl.
Diese Verbindung hat völlig neue Eigenschaften: sie ist ein kristalliner weißer Feststoff, der salzig schmeckt. Natrium ist ein Metall, das auf dem Wasser schwimmt und dabei heftig reagiert; es brennt mit gelber Flamme. Chlor ist ein grünliches Gas, das stechend riecht und ätzend wirkt. Man sieht der Verbindung also nicht an, was in ihr steckt.
Den Chemiker interessiert von jeher, welche Verbindung er vor sich hat und wie sie zusammengesetzt ist. Dazu hat er die chemische Analyse erfunden. Er nutzt dazu die Eigenschaften der Elemente aus: ein weißer Feststoff, der die Flamme gelb färbt, enthält z. B. Natrium. Wenn seine Lösung mit Silbernitrat einen weißlichen Niederschlag bildet, enthält er Chlor. Wenn beides Eintritt, handelt es sich mit einiger Sicherheit um Kochsalz.
Nun ist nicht alles so einfach. Eisen und Sauerstoff bilden mehrere Verbindungen: schwarzes Eisenoxid FeO, ein braunrotes Oxid Fe2O3 und ein ebenfalls schwarzes Fe3O4. Es reicht hier nicht zu wissen, welche Elemente in den drei Verbindungen enthalten sind, man muß auch wissen, in welchem Verhältnis sie enthalten sind: 1 : 1, 2 : 3 oder 3 : 4.
Es interessiert also die Frage: wenn x Fe-Atome und y O-Atome ein Oxid FexOy bilden, wie ist der Eisengehalt des Oxids Fe ⁄ (x · Fe + y · O).
- FeO enthält 2 · Fe ⁄ (Fe + O) =56 g ⁄ (56 g + 16 g) = 0,78 ⇒ 78 Gew-% Eisen,
- Fe2O3 enthält 3 · 56 g ⁄ (2 · 56 g + 3 · 16 g = 0,35 ⇒ 70 Gew-% Eisen,
- Fe3O4 enthält 72 Gew-% Eisen.
Man muß schon recht genau hinsehen, um die drei Oxide am Eisengehalt unterscheiden zu können.
Um den Eisengehalt einer Probe genau zu bestimmen, überführt man das darin enthaltene Eisen in eine Verbindung, die man genau kennt. Es bietet sich das Eisensulfid (FeS) an. Eine abgewogene Menge der Probe wird in Salzsäure aufgelöst, und mit Schwefelwasserstoff (H2S) fällt das Eisen als Eisensulfid aus. Das filtriert man ab, trocknet es und wägt es. Von der Probe wissen wir nun:
- das Gewicht der Probe,
- das Gewicht des Derivats FeS,
- das Verhältnis Fe : S im FeS.
Gesucht ist der Anteil des Eisens in der Probe in Prozent, um die drei Eisenoxide unterscheiden zu können.
In der Probe waren soviele Gramm Eisen, wie Gramm Eisen im FeS-Niederschlag enthalten sind: Fe ⁄ (Fe + S) = 56 ⁄ (56 + 32) = 64 %. Das Multipliziert mit dem gefundenen Gewicht an FeS gibt den Gewichtsanteil des Eisens in der Probe. Teilen wird diesen durch das Probengewicht, haben wir die gesuchten Gew-% Fe. Der Anteil Fe im FeS ist konstant, man nennt ihn Äquivalentgewicht. Es verhält sich also das Äquivalentgewicht von Eisen MGFe zum Gewicht des gefundenen FeS-Niederschlags GFeS, wie der Gewichtsanteil x des Eisens in Probe zum Probengewicht GP.
Das ist der klassische Dreisatz: wie gemacht für den Rechenschieber! Das fand auch William Hyde Wollaston, und er entwickelte 1813 den "Rechenschieber für Chemiker" und nannte ihn Synoptic Scale of Equivalents. Eine Beschreibung mit Abbildung und Anleitung aus dem Jahr 1832 habe ich bei Benjamin Scholz gefunden. Die letzten hergestellten chemischen Rechenschieber funktionierten genau nach diesem Prizip.
Vorgeschichte
Der Chemie wurden auf dem Ersten Weltkongress der Chemiker vom 03. bis 05. September 1860 in Karlsruhe die wesentlichen Impulse für die zukünftige Entwicklung zur Naturwissenschaft im heutigen Sinne gesetzt. Über 100 Chemiker aus aller Welt diskutierten die Ergebnisse der bis dahin bekannten Untersuchungen und stimmten die weiteren Forschungen ab. Hier wurden die Definitionen von u. a. "Element", "Verbindung", "Äquivalent" vorgeschlagen. Es zeichnete sich die "Analytische Chemie" als Kerngebiet der weiteren Forschungen ab. Und der 42 jährige Chemiker Carl Remigius Fresenius erkannte die Zeichen und gründete 1862 die erste Zeitschrift auf einem Spezialgebiet der Naturwissenschaften: die "Zeitschrift für Analytische Chemie" (sie erscheint noch heute als Fresenius Journal of Analytical Chemistry). Im Jahre 1869 publizierten Lothar Meyer und Dmitri Mendelejew unabhängig von einander ein "Periodensystem der (damals bekannten 65) Elemente". Nun konnten die Beziehungen der Elemente zueinander und ihre Eigenschaften systematisch untersucht werden. In meinem Studium hatte die "chemische Analytik" noch einen prominenten Platz.
Der interessante Teil der Chemie beschäftigt sich mit der Frage: wie beeinflusst die molekulare Zusammensetzung der Materie deren Eigenschaften, und wie kann man die Moleküle so verändern, dass die Materie daraus gewünschte Eigenschaften hat? Im Grunde läuft chemische Forschung also auf die Suche nach neuen Molekülen heraus, b.z.w. auf die Entwicklung von Methoden zur (industriellen) Herstellung von bekannten Molekülen. Da Atome und Moleküle unvorstellbar klein sind, kann man sie nicht einzeln bearbeiten, sondern nur in großer Zahl, in "wägbaren" Mengen.
Die Kunst des chemischen Rechnens wurde von Jeremias Benjamin Richter in seinen drei Bänden Stöchyometrie oder Meßkunst chymischer Elemente entwicklet. Aus dem zweiten Band Zweiter Theil welcher die angewandte Stöchyometrie enthält; für Mathematiker, Chymisten, Mineralogen und Pharmaceuten. habe ich den "Vorbericht." erfasst. Er gibt einen hübschen Überblick der Fragestellung — und eine Anleitung zum Rechnen mit Dezimalzahlen, die 1785 von Simon Stevin in einem Traktat vorgeschlagen worden waren. Joseph-Louis Proust und John Dalton fanden 1797 bzw. 1808 auf der Basis Richters Vorarbeiten die nach ihnen benannten Gesetze, wonach die Atome in immer den gleichen, ganzzahligen (Gewichts-) Verhältnissen zu Molekülen zusammentreten. Allgemein: zwei Atomarten A und B treten zu Molekülen AxBy zusammen, wobei x und y ganze Zahlen sind (1, 2, 3, …), und A und B sind die "Äquivalentgewichte". Die konnte man aus den beiden Gesetzen und einer Vielzahl von Verbindungen kann man Massenverhältnisse berechnen.
In der Chemie benutzt man daher "relative Atommassen". Heute werden die relativen Atommassen (willkürlich) auf das Kohlenstoffisotop mit der Atommasse 12 (12C) bezogen.
Der Physiker Amedeo Avogadro postulierte, dass gleiche Gasvolumina idealer Gase die gleiche Anzahl Moleküle enthalten. Joseph Loschmidt bestimmte die Anzahl zu 6,022 · 1023 (Loschmidtsche Zahl NL). Seit 1909 (auf Vorschlag Jean-Baptiste Perrins wird die Masse einer Substanz, die NL Moleküle enthält als "Mol" bezeichnet. Die Masse des "Mol" entspricht der Summe der Atommassen in den Molekülen.
Mit diesem Bezug von Masse (durch Wägen leicht zu bestimmen) und Anzahl Atome bzw. Moleküle wird in der Chemie gerechnet. Das Konzept des "Mol" ist zunächst ungewohnt, denn es hängt von der Atomart und der Molekülformel ab. Zum Beispiel 1 Mol Sauerstoff O2 entspricht 32 g, 1 Mol Chlor Cl2 dagegen 70 g; noch dazu nehmen beide Gase bei 0 °C und einem Druck von 1023 hPa ein Volumen von 22,4 Liter ein.
Das sind die Grundlagen des "chemischen" Rechnens.
Also: eine Verbindung besteht aus k Atomen des Elements X, l Atomen des Elements Y und n Atomen des Elements Z. Seine Summenformel schreibt man dann XkYlZn. Das Molekulargewicht M ist M = k · mX + l · mY + l · mZ, wobei mX das relative Atomgewicht des Elements X ist, etc..
Die Verbindung XkYlZn enthält somit (k · mX ⁄ M) · 100 Prozent des Elements X, (l · mY ⁄ M) · 100 Prozent des Elements Y, u. s. w..
Datenschutzerklärung